Плотность гидроксида натрия. Какие принять меры при получении ожога едким натром. Обширное использование в быту
Как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разьедать кожу, бумагу, стекло и вызывать сильные ожоги. До XVII века, щёлочью (фр. alkali ) называли также карбонаты натрия и калия. В французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия - кальцинированной содой (по растению Salsola Soda, из золы которого её добывали), а карбонат калия - поташем . В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium - калий.
Физические свойства
Гидроксид натрия
Термодинамика растворов
ΔH 0 растворения для бесконечно разбавленного водного раствора -44,45 кДж/моль.
Из водных растворов при 12,3 - 61,8 °C кристаллизуется моногидрат (сингония ромбическая), температура плавления 65,1 °C; плотность 1,829 г/см³; ΔH 0 обр −734,96 кДж/моль), в интервале от -28 до -24°С - гептагидрат, от -24 до -17,7°С - пентагидрат, от -17,7 до -5,4°С -тетрагидрат (α-модификация), от -5,4 до 12,3 °C. Растворимость в метаноле 23,6 г/л (t=28 °C), в этаноле 14,7 г/л (t=28 °C). NaOH·3,5Н 2 О (температура плавления 15,5 °C);
Химические свойства
(в целом такую реакцию можно представить простым ионным уравнением, реакция протекает с выделением тепла (экзотермическая реакция): OH - + H 3 O + → 2H 2 O. )
- с амфотерными оксидами которые обладают как основными, так и кислотными свойствами, и способностью реагировать с щелочами, как с твердыми при сплавлении:
ZnO + 2NaOH → Na 2 ZnO 2 + H 2 O
так и с растворами:
ZnO + 2NaOH (раствор) + H 2 O → Na 2 (раствор) +H 2
(Образующийся анион называется тетрагидроксоцинкат-ионом, а соль, которую можно выделить из раствора - тетрагидроксоцинкатом натрия. В аналогичные реакции гидроксид натрия вступает и c другими амфотерными оксидами.)
- с кислотными оксидами - с образованием солей; это свойство используется для очистки промышленных выбросов от кислотных газов (например: CO 2 , SO 2 и H 2 S):
2Na + + 2OH - + Cu 2+ + SO 4 2- → Cu(OH) 2 ↓+ Na 2 SO 4
Гидроксид натрия используется для осаждения гидроксидов металлов. К примеру, так получают гелеобразный гидроксид алюминия , действуя гидроксидом натрия на сульфат алюминия в водном растворе. Его и используют, в частности, для очистки воды от мелких взвесей.
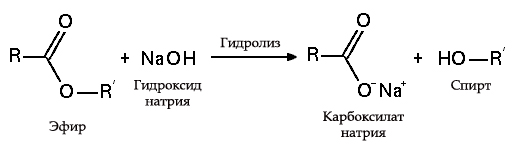
Гидролиз эфиров
- с жирами (омыление), такая реакция необратима, так как получающаяся кислота со щёлочью образует мыло и глицерин . Глицерин впоследствии извлекается из подмыльных щёлоков путем вакуум-выпарки и дополнительной дистилляционной очистки полученных продуктов. Этот способ получения мыла был известен на Ближнем Востоке с VII века:

Процесс омыления жиров
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла, в зависимости от состава жира.
HO-CH 2 -CH 2 ОН + 2NaOH → NaO-CH 2 -CH 2 -ONa + 2Н 2 O
2NaCl + 2H 2 О = H 2 + Cl 2 + 2NaOH,В настоящее время едкая щёлочь и хлор вырабатываются тремя электрохимическими методами. Два из них - электролиз с твёрдым асбестовым или полимерным катодом (диафрагменный и мембранный методы производства), третий - электролиз с жидким катодом (ртутный метод производства). В ряду электрохимических методов производства самым лёгким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути. Мембранный метод производства самый эффективный, наименее энергоёмкий и наиболее экологичный, но и самый капризный, в частности, требует сырьё более высокой чистоты.
Едкие щёлочи, полученные при электролизе с жидким ртутным катодом, значительно чище полученных диафрагменным способом. Для некоторых производств это важно. Так, в производстве искусственных волокон можно применять только каустик, полученный при электролизе с жидким ртутным катодом. В мировой практике используются все три метода получения хлора и каустика, при явной тенденции в сторону увеличения доли мембранного электролиза. В России приблизительно 35 % от всего выпускаемого каустика вырабатывается электролизом с ртутным катодом и 65 % - электролизом с твёрдым катодом (диафрагменный и мембранный методы).
Эффективность процесса производства рассчитывается не только по выходу едкого натра, но и по выходу хлора и водорода, получаемых при электролизе, соотношение хлора и гидроксида натрия на выходе 100/110, реакция протекает в следующих соотношениях:
1,8 NaCl + 0, 5 H 2 O + 2,8 МДж = 1,00 Cl 2 + 1,10 NaOH + 0,03 H 2 ,Основные показатели различных методов производства даны в таблице:
| Показатель на 1 тонну NaOH | Ртутный метод | Диафрагменный метод | Мембранный метод |
|---|---|---|---|
| Выход хлора % | 97 | 96 | 98,5 |
| Электроэнергия (кВт·ч) | 3 150 | 3 260 | 2 520 |
| Концентрация NaOH | 50 | 12 | 35 |
| Чистота хлора | 99,2 | 98 | 99,3 |
| Чистота водорода | 99,9 | 99,9 | 99,9 |
| Массовая доля O 2 в хлоре, % | 0,1 | 1-2 | 0,3 |
| Массовая доля Cl - в NaOH, % | 0,003 | 1-1,2 | 0,005 |
Технологическая схема электролиза с твёрдым катодом
Диафрагменный метод - Полость электролизёра с твёрдым катодом разделена пористой перегородкой - диафрагмой - на катодное и анодное пространство, где соответственно размещены катод и анод электролизёра. Поэтому такой электролизёр часто называют диафрагменным, а метод получения - диафрагменным электролизом . В анодное пространство диафрагменного электролизёра непрерывно поступает поток насыщенного анолита. В результате электрохимического процесса на аноде за счет разложения галита выделяется хлор, а на катоде за счет разложения воды - водород. Хлор и водород выводятся из электролизёра раздельно, не смешиваясь:
2Cl - − 2е = Cl 2 0 , H 2 O − 2e − 1/2 О 2 = H 2 .
При этом прикатодная зона обогащается гидроксидом натрия. Раствор из прикатодной зоны, называемый электролитическим щёлоком , содержащий неразложившийся анолит и гидроксид натрия, непрерывно выводится из электролизёра. На следующей стадии электролитический щёлок упаривают и доводят содержание в нём NaOH до 42-50 % в соответствии со стандартом. Галит и сульфат натрия при повышении концентрации гидроксида натрия выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или на стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией. Кристаллический галит (обратную соль) возвращают на электролиз, приготавливая из неё так называемый обратный рассол. Из него во избежание накапливания сульфата в растворах перед приготовлением обратного рассола извлекают сульфат. Убыль анолита возмещают добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов или растворением твёрдого галита. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния. Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Мембранный метод - аналогичен диафрагменному, но анодное и катодное пространства разделены катионообменной мембраной. Мембранный электролиз обеспечивает получение наиболее чистого каустика.
Технологическая схема электролиза .Основная технологическая стадия - электролиз, основной аппарат - электролитическая ванна, которая состоит из электролизёра, разлагателя и ртутного насоса, объединенных между собой коммуникациями. В электролитической ванне под действием ртутного насоса циркулирует ртуть, проходя через электролизёр и разлагатель. Катодом электролизёра служит поток ртути. Аноды - графитовые или малоизнашивающиеся. Вместе с ртутью через электролизёр непрерывно течёт поток анолита - раствор галита. В результате электрохимического разложения галита на аноде образуются ионы Cl - и выделяется хлор:
2 Cl - - 2е = Cl 2 0 ,
который отводится из электролизёра, а на ртутном катоде образуется слабый раствор натрия в ртути, так называемая амальгама :
Na + + е = Na 0 nNa + + nHg - = Na + HgАмальгама непрерывно перетекает из электролизёра в разлагатель. В разлагатель также непрерывно подаётся хорошо очищенная от примесей вода. В нем амальгама натрия в результате самопроизвольного электрохимического процесса почти полностью разлагается водой с образованием ртути, раствора каустика и водорода:
Na + Hg + Н 2 0 = NaOH + 1/2Н 2 + HgПолученный таким образом раствор каустика, являющийся товарным продуктом, не содержит примеси галита, вредной в производстве вискозы. Ртуть почти полностью освобождается от амальгамы натрия и возвращается в электролизер. Водород отводится на очистку. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесенные с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают двух- или трёхступенчатым процессом растворённый в нём хлор.
Лабораторные способы получения
В лаборатории гидроксид натрия получают химическими способами, которые имеют больше историческое, чем практическое значение.
Известковый способ получения гидроксида натрия заключается во взаимодействии раствора соды с известковым молоком при температуре около 80 °C . Этот процесс называется каустификацией; он описывается реакцией:
Na 2 C0 3 + Са (ОН) 2 = 2NaOH + CaC0 3В результате реакции образуется раствор гидроксида натрия и осадок карбоната кальция. Карбонат кальция отделяется от раствора, который упаривается до получения расплавленного продукта, содержащего около 92 % NaOH. Расплавленный NaOH разливают в железные барабаны, где он застывает.
Ферритный способ описывается двумя реакциями:
Na 2 C0 3 + Fe 2 0 3 = Na 2 0 Fe 2 0 3 + C0 2 (1) Na 2 0 Fe 2 0 3 -f H 2 0 = 2 NaOH + Fe 2 O 3 (2)(1) - процесс спекания кальцинированной соды с окисью железа при температуре 1100-1200°С. При этом образуется спек-феррит натрия и выделяется двуокись углерода. Далее спек обрабатывают (выщелачивают) водой по реакции (2); получается раствор гидроксида натрия и осадок Fe 2 O 3 , который после отделения его от раствора возвращается в процесс. Раствор содержит около 400 г/л NaOH. Его упаривают до получения продукта, содержащего около 92 % NaOH.
Химические методы получения гидроксида натрия имеют существенные недостатки: расходуется большое количество топлива, получаемый едкий натр загрязнен примесями, обслуживание аппаратов трудоемко. В настоящее время эти методы почти полностью вытеснены электрохимическим способом производства.
Рынок каустической соды
Мировое производство натра едкого, 2005 год| Производитель | Обьем производства, млн.тонн | Доля в мировом производстве |
|---|---|---|
| DOW | 6.363 | 11.1 |
| Occidental Chemical Company | 2.552 | 4.4 |
| Formosa Plastics | 2.016 | 3.5 |
| PPG | 1.684 | 2.9 |
| Bayer | 1.507 | 2.6 |
| Akzo Nobel | 1.157 | 2.0 |
| Tosoh | 1.110 | 1.9 |
| Arkema | 1.049 | 1.8 |
| Olin | 0.970 | 1.7 |
| Россия | 1.290 | 2.24 |
| Китай | 9.138 | 15.88 |
| Другие | 27.559 | 47,87 |
| Всего: | 57,541 | 100 |
ТР - твердый ртутный (чешуированный);
ТД - твердый диафрагменный (плавленый);
РР - раствор ртутный;
РХ - раствор химический;
РД - раствор диафрагменный.
| Наименование показателя | ТР ОКП 21 3211 0400 | ТД ОКП 21 3212 0200 | РР ОКП 21 3211 0100 | РХ 1 сорт ОКП 21 3221 0530 | РХ 2 сорт ОКП 21 3221 0540 | РД Высший сорт ОКП 21 3212 0320 | РД Первый сорт ОКП 21 3212 0330 |
|---|---|---|---|---|---|---|---|
| Внешний вид | Чешуирова- нная масса белого цвета. Допускается слабая окраска | Плавленая масса белого цвета. Допускается слабая окраска | Бесцветная прозрачная жидкость | Бесцветная или окрашенная жидкость. Допускается выкристалли- зованный осадок | Бесцветная или окрашенная жидкость. Допускается выкристалли- зованный осадок | Бесцветная или окрашенная жидкость. Допускается выкристалли- зованный осадок | |
| Массовая доля гидроксида натрия, %, не менее | 98,5 | 94,0 | 42,0 | 45,5 | 43,0 | 46,0 | 44,0 |
| Наименование предприятия | 2005 г. тыс.тонн | 2006 г. тыс.тонн | доля в 2005 г.% | доля в 2006 г.% |
|---|---|---|---|---|
| ОАО «Каустик» , Стерлитамак | 239 | 249 | 20 | 20 |
| ОАО «Каустик» , Волгоград | 210 | 216 | 18 | 18 |
| ОАО «Саянскхимпласт» | 129 | 111 | 11 | 9 |
| ООО «Усольехимпром» | 84 | 99 | 7 | 8 |
| ОАО «Сибур-Нефтехим» | 87 | 92 | 7 | 8 |
| ОАО «Химпром» , Чебоксары | 82 | 92 | 7 | 8 |
| ВОАО «Химпром» , Волгоград | 87 | 90 | 7 | 7 |
| ЗАО «Илимхимпром» | 70 | 84 | 6 | 7 |
| ОАО «КЧХК» | 81 | 79 | 7 | 6 |
| НАК «АЗОТ» | 73 | 61 | 6 | 5 |
| ОАО «Химпром», Кемерово | 42 | 44 | 4 | 4 |
| Итого: | 1184 | 1217 | 100 | 100 |
| Наименование предприятия | 2005 г. тонн | 2006 г. тонн | доля в 2005 г.% | доля в 2006 г.% |
|---|---|---|---|---|
| ОАО «Каустик» , Волгоград | 67504 | 63510 | 62 | 60 |
| ОАО «Каустик» , Стерлитамак | 34105 | 34761 | 31 | 33 |
| ОАО «Сибур-Нефтехим» | 1279 | 833 | 1 | 1 |
| ВОАО «Химпром» , Волгоград | 5768 | 7115 | 5 | 7 |
| Итого: | 108565 | 106219 | 100 | 100 |
(каустическая сода) представляет собой твердое белое вещество, имеющее вид гранул или плавленой массы, обладающее гигроскопическими свойствами. При растворении имеет свойство выделять тепло. За счет сильного разрушительного действия на ткани, кожу и прочие органические вещества каустическая сода (формула NaOH) имеет название "едкая щелочь" или "едкий натрий", а на производственных предприятиях - "каустик". В жидком состоянии, как правило, окрашенная или бесцветная жидкость, в которой может образовываться осадок.
Каустическая сода: применение
Соду каустическую (натрий едкий) используют для бытовых нужд, а также в разных отраслях промышленности. Это самая распространенная щелочь.
Каустическая сода применение нашла в следующих сферах:
- каустическая сода - зарегистрированная пищевая добавка Е524, которая используется для производства мороженого, шоколада, различных напитков, как размягчающее средство для маслин и др.
- в целлюлозно-бумажной промышленности (изготовление картона, разных видов бумаги, плит из древесного волокна, искусственного волокна и многого другого);
- для производства биодизельного топлива, которое изготовляется из растительных масел;
- в химической промышленности (для изготовления моющих средств, нейтрализации окислов и кислот, для титрования алюминия, для производства масел и прочего);
- в легкой промышленности (для отбеливания тканей, в производстве шелка);
- в автомобильном производстве (используют в изготовлении щелочных аккумуляторов);
- в пищевой промышленности (для промывки оборудования; обработки и производства продуктов питания).
Производство каустической соды
Самый распространенный способ получения едкого натрия - электролиз водного раствора галита (NaCL). Химическая реакция проходит с сопровождением выделения водорода и хлора.
Часто каустическая сода производится путем электролиза с использованием полимерных или асбестовых катодов (мембранные и диафрагменные методы), более редко получают путем электролиза с ртутным катодом.
К самому удобному методу относится ртутный способ производства, где катод - это металлическая ртуть.
При помощи высокого коэффициента перенапряжения на ртути водорода ионы натрия у катода разряжаются, и в итоге получается амальгама натрия, которая разлагается в горячей воде. В результате получается очень чистый NaOH, потому как в нем отсутствуют примеси. Однако этот метод считается очень вредным, поскольку применение металлической ртути вызывает загрязнение окружающей среды.
Мембранный и диафрагменный методы являются более эффективными, не требующими больших затрат. Именно их чаще всего применяют во всем мире.

Упаковка продукта
Каустическая сода, в зависимости от ее вида, может быть упакована различными способами. В твердом состоянии ее компонуют в стальные барабаны. Раствор каустической соды заливают в специальные автомобильные контейнеры и железнодорожные цистерны.

Хранение вещества
Жидкую соду хранят в помещениях в закрытых емкостях, устойчивых к действию щелочей. Твердый едкий натрий хранится в упакованном виде в закрытых неотапливаемых складах.
Транспортировка
Перевозят каустическую соду при помощи транспорта (железнодорожного, автомобильного и водного). При проведении доставки твердого едкого натрия данный продукт упаковывают в мешки, а жидкое вещество перевозят в специальных железнодорожных цистернах и емкостях. При транспортировке каустической соды следует избегать нагревания и попадания на нее влаги.
Гарантийный срок хранения едкого натрия с даты изготовления - 1 год.

Описание
В мире добывается и используется в течение года более 58 млн. тонн каустической соды. Данное вещество имеет удельный вес 2,13, может хорошо растворяться в воде (при температуре 0 градусов - 43%), но не растворимо в дихлорэтане. Натрий едкий идет на изготовление дегазирующего раствора №2, кроме того, вещество используют для дегазации местности. Аммиачно-щелочной раствор №2 состоит из таких компонентов:
- натрия едкого (2%);
- аммиака (20%);
- моноэтаноламина (5%).
Данным раствором проводят дегазацию боевой техники, военного транспорта, разного вооружения, которые оказались заражены такими отравляющими веществами, как, например, зарин.
Аммиак и моноэтаноламин используют как дегазирующие вещества, а также для снижения температуры замерзания состава до - 40°C. Данный раствор хранят в железных бочках, объем которых - 100 и 250 л, в них и происходит транспортировка в расположение воинских частей и на производства.
Концентрированный раствор способен разрушать обувь и ткани, а также разъедать кожу людей.
Меры предосторожности
При обращении с данным веществом нельзя забывать об опасности, которую оно может в себе содержать. Каустическая сода (формула NaOH) едкая, коррозионно активная, относится ко 2 классу опасности. При работе с ней нужно обязательно соблюдать все необходимые меры предосторожности. Попадание вещества в глаза или на кожу может вызвать серьезный химический ожог.
При попадании натрия едкого на слизистую поверхность нужно немедленно пораженный участок промыть проточной водой, а в случае попадания на кожу протереть раствором уксусной кислоты.
- брызгозащитные химические очки (для защиты глаз);
- резиновые перчатки (для защиты рук);
- прорезиненный костюм или спецодежду, пропитанную винилом (для защиты туловища).
Физические свойства
Гидрат окиси натрия NaOH - белое твердое вещество. Если оставить кусок едкого натра на воздухе, то он вскоре расплывается, так как притягивает влагу из воздуха. Едкий натр хорошо растворяется в воде, при этом выделяется большое количество теплоты. Раствор едкого натра мылок на ощупь.
Термодинамика растворов
ΔH 0 растворения для бесконечно разбавленного водного раствора −44,45 кДж/моль.
Из водных растворов при 12,3-61,8 °C кристаллизуется моногидрат (сингония ромбическая), температура плавления 65,1 °C; плотность 1,829 г/см³; ΔH 0 обр −425,6 кДж/моль), в интервале от −28 до −24 °C - гептагидрат, от −24 до −17,7 °C - пентагидрат, от −17,7 до −5,4 °C - тетрагидрат (α-модификация), от −5,4 до 12,3 °C. Растворимость в метаноле 23,6 г/л (t = 28 °C), в этаноле 14,7 г/л (t = 28 °C). NaOH·3,5Н 2 О (температура плавления 15,5 °C);
Химические свойства
(1) H 2 S + 2NaOH = Na 2 S + 2H 2 O (при избытке NaOH)
(2) H 2 S + NaOH = NaHS + H 2 O (кислая соль, при отношении 1:1)
(в целом такую реакцию можно представить простым ионным уравнением, реакция протекает с выделением тепла (экзотермическая реакция): OH − + H 3 O + → 2H 2 O. )
- с амфотерными оксидами которые обладают как основными, так и кислотными свойствами, и способностью реагировать с щелочами, как с твёрдыми при сплавлении:
ZnO + 2NaOH → Na 2 ZnO 2 + H 2 O
так и с растворами:
ZnO + 2NaOH (раствор) + H 2 O → Na 2 (раствор)
(Образующийся анион называется тетрагидроксоцинкат-ионом, а соль, которую можно выделить из раствора - тетрагидроксоцинкатом натрия. В аналогичные реакции гидроксид натрия вступает и c другими амфотерными оксидами.)
Al(OH) 3 + 3NaOH = Na 3
2Na + + 2OH − + Cu 2+ + SO 4 2− → Cu(OH) 2 ↓+ Na 2 SO 4
Гидроксид натрия используется для осаждения гидроксидов металлов. К примеру, так получают гелеобразный гидроксид алюминия , действуя гидроксидом натрия на сульфат алюминия в водном растворе, при этом избегая избытка щёлочи и растворения осадка. Его и используют, в частности, для очистки воды от мелких взвесей.
4Р + 3NaOH + 3Н 2 О → РН 3 + 3NaH 2 РО 2 .
3S + 6NaOH → 2Na 2 S + Na 2 SO 3 + 3H 2 O
Гидролиз эфиров
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла, в зависимости от состава жира.
HO-CH 2 -CH 2 ОН + 2NaOH → NaO-CH 2 -CH 2 -ONa + 2Н 2 O
Анод : 2Cl − - 2е − → Cl 2 - основной процесс 2H 2 O - 2e - → O 2 +4H + 6СlО - + 3Н 2 О - 6е - → 2СlО 3 - + 4Сl - + 1,5O 2 + 6Н + Катод : 2H 2 O + 2e − → H 2 + 2OH − - основной процесс СlО - + Н 2 О + 2е - → Сl - + 2ОН - СlО 3 - + 3Н 2 O + 6е - → Сl - + 6OН -В качестве анода в диафрагменных электролизерах может использоваться графитовый или угольный электроды. На сегодня их в основном заменили титановые аноды с окисно-рутениево-титановым покрытием (аноды ОРТА) или другие малорасходуемые.
На следующей стадии электролитический щёлок упаривают и доводят содержание в нём NaOH до товарной концентрации 42-50 % масс. в соответствии со стандартом.
Na + + е = Na 0 nNa + + nHg − = Na + HgАмальгама непрерывно перетекает из электролизёра в разлагатель амальгамы. В разлагатель также непрерывно подаётся высоко очищенная вода. В нём амальгама натрия в результате самопроизвольного химического процесса почти полностью разлагается водой с образованием ртути, раствора каустика и водорода:
Na + Hg + Н 2 O = NaOH + 1/2Н 2 + HgПолученный таким образом раствор каустика, являющийся товарным продуктом, практически не содержит примесей. Ртуть почти полностью освобождается от натрия и возвращается в электролизер. Водород отводится на очистку.
Однако, полная очистка раствора щелочи от остатков ртути практически не возможна, поэтому этот метод сопряжен с утечками металлической ртути и её паров.
Растущие требования к экологической безопасности производств и дороговизна металлической ртути ведут к постепенному вытеснению ртутного метода методами получения щелочи с твердым катодом, в особенности мембранным методом.
Лабораторные методы получения
В лаборатории гидроксид натрия иногда получают химическими способами, но чаще используется небольшой электролизер диафрагменного или мембранного типа.
Рынок каустической соды
Мировое производство натра едкого, 2005 год| Производитель | Объём производства, млн.тонн | Доля в мировом производстве |
|---|---|---|
| DOW | 6.363 | 11.1 |
| Occidental Chemical Company | 2.552 | 4.4 |
| Formosa Plastics | 2.016 | 3.5 |
| PPG | 1.684 | 2.9 |
| Bayer | 1.507 | 2.6 |
| Solvay | 1.252 | 2.2 |
| Akzo Nobel | 1.157 | 2.0 |
| Tosoh | 1.110 | 1.9 |
| Arkema | 1.049 | 1.8 |
| Olin | 0.970 | 1.7 |
| Россия | 1.290 | 2.24 |
| Китай | 9.138 | 15.88 |
| Другие | 27.559 | 47,87 |
| Всего: | 57,541 | 100 |
ТР - твёрдый ртутный (чешуированный);
ТД - твёрдый диафрагменный (плавленый);
РР - раствор ртутный;
РХ - раствор химический;
РД - раствор диафрагменный.
| Наименование показателя | ТР ОКП 21 3211 0400 | ТД ОКП 21 3212 0200 | РР ОКП 21 3211 0100 | РХ 1 сорт ОКП 21 3221 0530 | РХ 2 сорт ОКП 21 3221 0540 | РД Высший сорт ОКП 21 3212 0320 | РД Первый сорт ОКП 21 3212 0330 |
|---|---|---|---|---|---|---|---|
| Внешний вид | Чешуированная масса белого цвета. Допускается слабая окраска | Плавленая масса белого цвета. Допускается слабая окраска | Бесцветная прозрачная жидкость | Бесцветная или окрашенная жидкость. Допускается выкристаллизованный осадок | Бесцветная или окрашенная жидкость. Допускается выкристаллизованный осадок | Бесцветная или окрашенная жидкость. Допускается выкристаллизованный осадок | |
| Массовая доля гидроксида натрия, %, не менее | 98,5 | 94,0 | 42,0 | 45,5 | 43,0 | 46,0 | 44,0 |
| Наименование предприятия | 2005 г. тыс.тонн | 2006 г. тыс.тонн | доля в 2005 г.% | доля в 2006 г.% |
|---|---|---|---|---|
| ОАО «Каустик» , Стерлитамак | 239 | 249 | 20 | 20 |
| ОАО «Каустик» , Волгоград | 210 | 216 | 18 | 18 |
| ОАО «Саянскхимпласт» | 129 | 111 | 11 | 9 |
| ООО «Усольехимпром» | 84 | 99 | 7 | 8 |
| ОАО «Сибур-Нефтехим» | 87 | 92 | 7 | 8 |
| ОАО «Химпром» , Чебоксары | 82 | 92 | 7 | 8 |
| ВОАО «Химпром» , Волгоград | 87 | 90 | 7 | 7 |
| ЗАО «Илимхимпром» | 70 | 84 | 6 | 7 |
| ОАО «КЧХК» | 81 | 79 | 7 | 6 |
| НАК «АЗОТ» | 73 | 61 | 6 | 5 |
| ОАО «Химпром», Кемерово | 42 | 44 | 4 | 4 |
| Итого: | 1184 | 1217 | 100 | 100 |
| Наименование предприятия | 2005 г. тонн | 2006 г. тонн | доля в 2005 г.% | доля в 2006 г.% |
|---|---|---|---|---|
| ОАО «Каустик» , Волгоград | 67504 | 63510 | 62 | 60 |
| ОАО «Каустик» , Стерлитамак | 34105 | 34761 | 31 | 33 |
| ОАО «Сибур-Нефтехим» | 1279 | 833 | 1 | 1 |
| ВОАО «Химпром» , Волгоград | 5768 | 7115 | 5 | 7 |
| Итого: | 108565 | 106219 | 100 | 100 |
Применение
Биодизельное топливо
Получение биодизеля
Едкий натр применяется во множестве отраслей промышленности и для бытовых нужд:
- Каустик применяется в целлюлозно-бумажной промышленности для делигнификации (сульфатный процесс) целлюлозы, в производстве бумаги , картона , искусственных волокон, древесно-волоконных плит.
- Для омыления жиров при производстве мыла , шампуня и других моющих средств . В древности во время стирки в воду добавляли золу, и, по-видимому, хозяйки обратили внимание, что если зола содержит жир, попавший в очаг во время приготовления пищи, то посуда хорошо моется. О профессии мыловара (сапонариуса) впервые упоминает примерно в 385 г. н. э. Теодор Присцианус. Арабы варили мыло из масел и соды с VII века, сегодня мыла производятся тем же способом, что и 10 веков назад. В настоящее время продукты на основе гидроксида натрия (с добавлением гидроксида калия, нагретые до 50-60 градусов Цельсия, применяются в сфере промышленной мойки для очистки изделий из нержавеющей стали от жира и других масляных веществ, а также остатков механической обработки.
- В химических отраслях промышленности - для нейтрализации кислот и кислотных окислов, как реагент или катализатор в химических реакциях, в химическом анализе для титрования , для травления алюминия и в производстве чистых металлов , в нефтепереработке - для производства масел.
- Для изготовления биодизельного топлива - получаемого из растительных масел и используемого для замены обычного дизельного топлива. Для получения биодизеля к девяти массовым единицам растительного масла добавляется одна массовая единица спирта (то есть соблюдается соотношение 9:1), а также щелочной катализатор (NaOH). Полученный эфир (главным образом линолевой кислоты) отличается хорошей воспламеняемостью, обеспечиваемой высоким цетановым числом. Цетановое число условная количественная характеристика самовоспламеняемости дизельных топлив в цилиндре двигателя (аналог октанового числа для бензинов). Если для минерального дизтоплива характерен показатель в 50-52 %, то метиловый эфир уже изначально соответствует 56-58 % цетана. Сырьем для производства биодизеля могут быть различные растительные масла: рапсовое , соевое и другие, кроме тех, в составе которых высокое содержание пальмитиновой кислоты (пальмовое масло). При его производстве в процессе этерификации также образуется глицерин который используется в пищевой, косметической и бумажной промышленности, либо перерабатывается в эпихлоргидрин по методу Solvay .
- В качестве агента для растворения засоров канализационных труб , в виде сухих гранул или в составе гелей . Гидроксид натрия дезагрегирует засор и способствует лёгкому продвижению его далее по трубе.
- В гражданской обороне для дегазации и нейтрализации отравляющих веществ, в том числе зарина , в ребризерах (изолирующих дыхательных аппаратах (ИДА), для очистки выдыхаемого воздуха от углекислого газа.
- Гидроксид натрия также используется в сочетании с цинком для фокуса . Медную монету кипятят в растворе гидроксида натрия в присутствии гранул металлического цинка, через 45 секунд, цвет копейки станет серебристым. После этого копейку вынимают из раствора и нагревают в пламени горелки, где она, практически моментально становится «золотой». Причины этих изменений заключается в следующем: ионы цинка вступают в реакцию с гидроксидом натрия (в недостатке) с образованием Zn (OH) 4 2− - который при нагревании разлагается до металлического цинка и осаждается на поверхность монеты. А при нагревании цинк и медь образуют золотистый сплав - латунь .
- Гидроксид натрия также используется для мойки пресс-форм автопокрышек.
- Гидроксид натрия также используется для нелегального производства метамфетаминов и других наркотических средств.
- В приготовлении пищи:
для мытья и очистки фруктов и овощей от кожицы, в производстве шоколада и какао, напитков, мороженого, окрашивания карамели, для размягчения маслин и придания им чёрной окраски, при производстве хлебобулочных изделий. Зарегистрирован в качестве пищевой добавки E524
.
Некоторые блюда готовятся с применением каустика:- Лютефиск - скандинавское блюдо из рыбы - сушёная треска вымачивается 5-6 дней в едкой щёлочи и приобретает мягкую, желеобразную консистенцию.
- Брецель - немецкие крендели - перед выпечкой их обрабатывают в растворе едкой щёлочи, которая способствует образованию уникальной хрустящей корочки.
- В косметологии для удаления ороговевших участков кожи: бородавок, папиллом.
Меры предосторожности при обращении с гидроксидом натрия
Гидроксид натрия - едкое и коррозионноактивное вещество . Оно относится к веществам второго класса опасности . Поэтому при работе с ним требуется соблюдать осторожность. При попадании на кожу, слизистые оболочки и в глаза образуются серьёзные химические ожоги . Попадание в глаза вызывает необратимые изменения зрительного нерва (атрофию), и, как следствие, потерю зрения. При контакте слизистых поверхностей с едкой щёлочью необходимо промыть поражённый участок струей воды, а при попадании на кожу слабым раствором уксусной кислоты . При работе с едким натрием рекомендуется следующие защитные средства : химические брызгозащитные очки для защиты глаз, резиновые перчатки или перчатки с прорезиненной поверхностью для защиты рук, для защиты тела - химически-стойкая одежда пропитанная винилом или прорезиненные костюмы.
ПДК гидроксида натрия в воздухе 0,5 мг/м³.
Литература
- Общая химическая технология. Под ред. И. П. Мухленова. Учебник для химико-технологических специальностей вузов. - М.: Высшая школа.
- Основы общей химии, т. 3, Б. В. Некрасов. - М.: Химия, 1970.
- Общая химическая технология. Фурмер И. Э., Зайцев В. Н. - М.: Высшая школа, 1978.
- Приказ Минздрава РФ от 28 марта 2003 г. N 126 «Об утверждении Перечня вредных производственных факторов, при воздействии которых в профилактических целях рекомендуется употребление молока или других равноценных пищевых продуктов».
- Постановление Главного государственного санитарного врача РФ от 4 апреля 2003 г. N 32 «О введении в действие Санитарных правил по организации грузовых перевозок на железнодорожном транспорте. СП 2.5.1250-03».
- Федеральный закон от 21.07.1997 N 116-ФЗ «О промышленной безопасности опасных производственных объектов » (с изменениями на 18 декабря 2006 года).
- Приказ МПР РФ от 2 декабря 2002 г. N 786 «Об утверждении федерального классификационного каталога отходов» (с изм. и доп. от 30 июля 2003 г.).
- Постановление Госкомтруда СССР от 25.10.1974 N 298/П-22 «Об утверждении списка производств, цехов, профессий и должностей с вредными условиями труда, работа в которых дает право на дополнительный отпуск и сокращённый рабочий день» (с изменениями на 29 мая 1991 года).
- Постановление Минтруда России от 22.07.1999 N 26 «Об утверждении типовых отраслевых норм бесплатной выдачи специальной одежды, специальной обуви и других средств индивидуальной защиты работникам химических производств».
- Постановление Главного государственного санитарного врача РФ от 30.05.2003 N 116 О введении в действие ГН 2.1.6.1339-03 «Ориентировочные безопасные уровни воздействия (ОБУВ) загрязняющих веществ в атмосферном воздухе населённых мест».(с изменениями на 3 ноября 2005 года).
| Растворимость кислот , оснований и солей в воде | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Существует три разновидности соды: пищевая, кальцинированная и каустическая. Если по поводу первой – всем известны ее свойства и химическая формула, то последние две имеют совершенно другие характеристики. Что такое каустическая сода, ее применение в быту, чем она опасна и полезна – в этой статье.
Каустическая сода – это распространенная и самая сильная щелочь
Свойства
Формула каустической соды – NaOH. Она имеет белый насыщенный цвет и хорошо растворяется в воде. Еще ее могут называть каустика или едкий натр, она бывает в растворенном и в твердом виде. В твердом состоянии ее транспортировка происходит в мешках, а в жидком перевозят в специальных емкостях. Что такое сода каустическая, очень хорошо знают в разных отраслях промышленности, даже в медицине она занимает определенное место. Но наряду с ее полезными свойствами, имеются также и негативные последствия ее применения.
Засоры канализаций
Свойства едкого натра широко используются в разных видах промышленности. Из него изготавливают минеральные удобрения, используют для прочистки канализации. При проблеме засорения канализационных труб эффективным средством для их очищения становится едкий натр. Для чистки канализации предлагается несколько вариантов:
- 4 ложки каустической соды засыпать в отверстие трубы, затем залить 300 мл кипятка. Когда пройдет 2 часа – промыть большим количеством воды.
- Уксус и сода – 1:1. По 130 грамм каждого вещества залить в канализацию, пока не начнется образование пены. После этого лучше на 2 часа закрыть отверстие трубы пробкой. По истечении нужного времени промыть кипятком.
- Смешать 7 литров воды и 4 килограмма каустика. Залить все в канализационную трубу − такая жидкая смесь очень эффективный вариант для промывки труб.
Каустическая сода очень часто используется для чистки канализации, она наилучший вариант для удаления засорений в трубах различного характера.
Применение для чистки канализации каустика особенно эффективно в многоэтажных домах, квартирах, где по-другому восстановить проходимость трубы очень проблематично.
Данное щелочное вещество также используют и для других бытовых целей. Жидкий раствор каустической соды почистит не только канализацию, но и старинные монеты, которые потеряли свой вид из-за длительного хранения.
Использование в агрономии
В случае увеличения количества соды можно навредить растениям, поэтому стоит четко соблюдать дозы и рецептуру. Чтобы не нарушать обмен веществ в почве, нужно обрабатывать только в зоне, пораженной вредителями.
Рецептура с использованием едкого натра применяется многими агрономами для борьбы с самыми разными вредителями. Наличие гидроокиси натрия в составе средства для обработки избавляет от многих грибковых заболеваний растений (мучнистой росы, фитофтороза и других). Это во многих случаях позволяет дешево и результативно повысить урожайность.
 Сода каустическая известна как технический едкий натрий и каустик, её выпускают в жидком и твердом виде
Сода каустическая известна как технический едкий натрий и каустик, её выпускают в жидком и твердом виде Когда урожай в теплицах уже собран, едкий натр также может понадобиться для обработки поверхности теплиц. Он предотвращает грибковые наслоения, образовавшиеся за время выращивания растений. Щелочь отлично дезинфицирует поверхности и препятствует размножению микроорганизмов.
Накипь и нагар отчистит едкий натр
Накипь, нагар, старый жир на посуде или в печи – все отчистит гидроокись натрия. Чтобы почистить загрязненную поверхность, необходимо соблюдать пропорции соединения щелочи и обычного моющего средства. Нужно развести соду с жидким моющим 1:1, добавить немного воды до образования однородной, но не совсем жидкой массы. Затем нанести на поверхность на половину часа. После этого смыть все тщательно водой. Применение каустической соды должно быть осторожным и внимательным, чтобы используя ее не нанести вред здоровью.
Делайте все манипуляции только в резиновых перчатках, чтобы не получить ожог на коже.
Не торопитесь и будьте осторожны. В случае получения ожога поместите пораженный участок кожи под сильную струю проточной воды на 10 минут и затем наложите бинт с уксусным 5% раствором. Затем обязательно следует обратиться к врачу хирург или комбустиологу.
Приготовление домашнего мыла
Едкий натр также нашел свое применение при изготовлении мыла в домашних условиях. Для этого его растворяют в очищенной воде, а затем добавляют разогретые эфирные масла. Применять щелочь нужно осторожно, чтобы не нанести повреждений кожным покровам.
После застывания полученной массы, ее размещают в подготовленные заранее формочки и оставляют на несколько дней. Такое мыло значительно дешевле, чем купленное в магазине.
Техника безопасности при использовании каустической соды
Щелочь всегда пользовалась спросом в разных отраслях промышленности. Без нее трудно представить промывку канализационных труб, или профилактическую дезинфекцию теплиц в сельскохозяйственной отрасли. В то время, когда существует масса промышленных химических веществ, используемых для борьбы с разными видами вредителей, каустик является недорогим и эффективным вариантом.
 Каустическую соду используют для изготовления минерального удобрения, биотоплива и в целлюлозно-бумажной отрасли
Каустическую соду используют для изготовления минерального удобрения, биотоплива и в целлюлозно-бумажной отрасли Однако пользоваться каустической содой следует очень осторожно. Инструкция по применению едкого натра включает следующие пункты:
- Пользуясь каустической содой, всегда нужно надевать резиновые перчатки, очки, плотную одежду, чтобы избежать попадания опасного вещества на кожу и получения при этом ожога.
- При чистке эмалированных и оцинкованных поверхностей нужно соблюдать рецептуру и пропорции соединения соды с водой или другими веществами.
- Хранить едкий натр необходимо в недоступном для детей месте в емкости с плотно закрытой крышкой.
Какие принять меры при получении ожога едким натром
Никто не застрахован на 100% от ошибок и неосторожности. Даже при соблюдении техники безопасности, при определенном стечении обстоятельств, можно случайно получить увечье кожи или слизистой во время использования каустика. В таком случае нужно сделать следующее:
- При попадании щелочи на слизистую – промыть 2% борной кислотой и ополоснуть проточной водой пораженный участок или глаза. Обязательно обратиться к врачу.
- При поражении участка кожи необходимо обработать его 5% уксусным раствором, и опять же обратиться в больницу.
Независимо от того, насколько легким будет ожог или повреждение глаз и слизистой – обращаться к врачу обязательно! После установленного врачом-специалистом диагноза нужно следовать дальнейшим действиям в отношении лечения.
Приобретение каустической соды
Купить щелочь или каустическую соду, можно в торговых точках, которые занимаются реализацией хозяйственных товаров (сантехника, стройматериалы, инвентарь).
В интернете подобного вида вещества также продаются, это можно использовать в случае, если у человека нет возможности тратить время на походы в магазины. Едкий натр очень универсален в своем применении, но, главное, – это соблюдение его инструкции по применению.
Применение каустической соды в быту обусловлено одним из ее свойств – нейтрализовать жиры и другие органические загрязнения. Именно способность растворять заторы из грязи и органических накоплений помогает справиться с очисткой канализации в частном секторе и многоквартирных домах. Кроме того, едкий натр (каустическая сода, гидроксид натрия, каустик) используется и для приготовления мыла своими руками в домашних условиях.
Очистка сливных труб и канализации
Существует два способа прочистки стока в умывальнике, ванне или душевой кабине, а также туалета или канализационной системы в частном доме. Первый больше подходит для прочистки стоков в системе канализации частного дома, второй – для очищения сифонов и сливных стояков в многоэтажках. Инструкция по применению, 1-й вариант:
- 2 кг каустической соды заливают холодной водой (4 л);
- полученный раствор выливают в канализацию;
- около часа нежелательно сливать воду: в это время едкий натр расщепляет жиры и другую органику.
- по истечении часа заливают воду (12-15 литров) с температурой 85-90 ºC.
При регулярной прочистке канализационных труб таким методом в доме гарантированно не будет неприятного запаха из труб, который появляется благодаря разложению остатков пищи и других биологических веществ. Инструкция по применению, 2-й способ:
- в горловину мойки или ванны засыпается до 150 г каустика;
- далее на порошок осторожно выливается до 2 литров горячей воды;
- через 5-10 минут горячая вода заливается повторно;
- около часа нельзя допускать попадания в горловину воды.
Едкий натр можно использовать после очистки труб кислотными веществами для нейтрализации агрессивного воздействия.

Чистка кастрюль
Так как гидроксид натрия хорошо справляется с жировыми загрязнениями, его используют для , кастрюль и другой кухонной утвари. Стоит сразу заметить, что такое применение не подходит для посуды из алюминия или тефлона. зато эмалированные, чугунные и стальные кастрюли доводит до идеального состояния. Для такой процедуры необходимо:
- в большую металлическую емкость залить воду (не менее 10 литров);
- всыпать туда едкий натр (200 г);
- добавить 1 брусок натертого на крупной терке хозяйственного мыла;
- влить 150 г канцелярского клея (жидкого стекла);
- хорошо размешать все и вложить в полученную смесь посуду;
- довести до кипения и держать на небольшом огне еще 2 часа;
- достать очищенную посуду и хорошо вымыть под проточной водой.
Таким же способом можно бороться с застарелым жиром на тарелках, только время кипячения сокращается до 10 минут.

Мыловарение
Каустик используется еще в одной области — для мыловарения. Его применение является обязательным, так как едкий натр — главный ингредиент в составе мыла:
- каустическая сода;
- растительное масло;
- эфирное масло;
- очищенная (дистиллированная) вода.
Существует множество рецептов мыла, в которых разнятся пропорции и добавляются специфические составляющие (в этом и состоит секрет мыловарения), но, используя основные ингредиенты, можно поэкспериментировать и приготовить мыло своими руками. Для этого каустик соединяют с водой, вводят в раствор растительное и эфирное масло. Смешивают составляющие до получения однородной массы, после чего выливают ее в формочки, где она застывает в течение суток.
Для косметических целей нужен едкий натр с высокой степенью очистки. Его можно приобрести в магазинах для мыловаров.

Хранение каустика и меры предосторожности
Чтобы разобраться, как правильно хранить едкий натр в домашних условиях, нужно выяснить, чем он является. Что такое каустическая сода? Прежде всего, это химическое вещество – сильная щелочь, вызывающая ожоги. Поэтому и раствор, и порошок необходимо держать в местах, недоступных для детей, в плотно закрытой таре с соответствующим ярлыком. Также каустик относится к горючим и взрывоопасным веществам, следовательно, он должен находиться вдали от нагревательных приборов и источников открытого огня.
Каустическую соду хранят в герметичной таре: порошок в бумажных мешках или полиэтиленовых банках, а жидкость в таре из плотного полиэтилена с резиновой пробкой. Срок хранения и жидкости, и гранул – 12 месяцев. Самостоятельно приготовленный 3%-й раствор также может хранится до 12 месяцев, однако перед использованием нужно проверить, не образовался ли осадок. Если в растворе наблюдаются хлопья, возможно, произошло преобразование в карбонат калия и он утратил свои свойства. Прозрачность или непрозрачность тары на свойства каустика никак не влияет.
Работая с гидроксидом натрия, необходимо соблюдать меры предосторожности:
- работать в резиновых перчатках;
- защищать глаза и слизистые оболочки от попадания химического вещества;
- не допускать попадания внутрь.
Если же каустик все же попал на кожу, нужно сразу промыть ее проточной водой. При случайном приеме внутрь или попадании в глаза лучше сразу же обратится к врачу, так как это может вызвать серьезные проблемы со зрением (отмирание тканей роговицы) или ожог гортани и пищевода, а также желудка.

Еще немного разных фактов
Каустик в быту находит применение и для других целей.
- Для дезинфекции в подсобных хозяйствах при опасных инфекционных заболеваниях у скота помещения обрабатывают 4%-м раствором едкого натра. Животных на время обработки выводят.
- При очистке металлической поверхности от ржавчины кислотой каустик является основным ингредиентом для пассивации. После обработки кислотными растворами металл обрабатывают смесью формалина, каустической соды, аммония и воды.
- Для удаления трудновыводимых жировых пятен или пятен от мазута с одежды. Вещи замачиваются 2 часа в воде с добавлением 2%-го раствора гидроксида натрия – 1 ст. ложка на литр воды. После этого стираются обычным способом. Если стирка ручная, обязательно должны надеваться резиновые перчатки.
Внимание!
Способ очистки от пятен каустической содой не походит для шелковых и шерстяных тканей. В 10%-м растворе каустика они растворяются без остатка, но и меньшая концентрация принесет этим тканям ощутимый ущерб.




